Une protéine dans la soupe ? (III e partie)

Résumé : À travers l'exemple de l'insuline et les relations d'une hormone avec son récepteur, Louis finit par donner la certitude à son fils Jean que la vie, d’une complexité qui défie l’imagination, ne peut pas surgir de peptides formés et réunis par hasard, fût-ce après des milliards d'années d'attente. Les évolutionnistes devraient comprendre que l’idée d’un « hasard organisateur » aveugle est irrationnelle, voire absurde. C’est la raison et l’évidence qui nous montrent l’Intelligence créatrice à l’œuvre.
J : Papa ! tu m'avais promis un exemple pour parler des modifications post-traductionnelles. Pourrais-tu me dire, avant, quelques mots sur le hasard, qui semble bien puissant pour tout expliquer ?
L : Des scientifiques pensent que le mouvement des particules est aléatoire, ce qui amène la question du hasard.
Insuline.
Selon son étymologie le mot hasard a trois sens :
le premier provient de l'arabe « jeu de dés » . Il renvoie à l'image d'un jeu de hasard. On est alors dans l'artificiel et le mathématisable. Le hasard amène donc très vite à un calcul mathématique de probabilités. Jacques Monod écrit dans Le Hasard et la Nécessité que le hasard est la raison d'être des choses et que nous sommes l'expression de combinaison de molécules aléatoires et contingentes. Il fonde ainsi l'origine de la vie sur une explication probabiliste, un jeu aléatoire. Comme il y a toujours un 1 après la virgule et des 0 plus ou moins nombreux, les probabilités pourraient laisser accroire qu'il y a toujours une chance que l'événement se soit produit.
Mais la nature ne joue pas aux dés. Il existe un déterminisme dans la nature que nous constatons puisque nous pouvons établir des lois physiques…
La vérité est l'adéquation de l'intellect à la réalité. Du fait de la complexité du réel et de nos connaissances partielles, il ne faut pas s'étonner si parfois les observations scientifiques sont déconcertantes et obligent les savants à remanier leur discipline.
Lorsque l’on considère notre monde vivant et sa diversité, on a largement dépassé le seuil d'impossibilité : une somme de probabilités trop faibles pour qu'il existe tel qu'il est !
le deuxième sens provient du latin casus , « chute, arrivée fortuite, accident » [ Gaffiot ]. Il fait référence au devenir naturel. Ce qui arrive fortuitement arrive par hasard. La préposition « par » signifie « cause ». Le hasard serait une explication.
le troisième, du grec τύχη tuchê , « ce que l’homme atteint par la décision des dieux, sort, succès » [ Bailly ] », avec un sens mythologique : la fortune. C'est le sort donné par les dieux aux hommes. Il ne dépend pas de nous. Il n'y a pas de hasard ; nous sommes soumis à la nécessité, à la volonté des dieux.
J : Qu'est-ce que je signifie quand je dis que ce qui m'arrive, m'arrive par hasard ?
L : Le hasard est une cause per accidens dit la philosophie. Ce qui t'arrive par hasard arrive rarement , dans un petit nombre de cas.
Ce qui t'arrive par hasard survient dans une action qui a une intention, une finalité . C'est la rencontre indéterminée de deux événements ou séries causales déterminées . Le hasard est d'abord un événement.
Voici un exemple. Le mois dernier, une tuile est tombée à côté de toi, sans doute détachée du toit par le vent alors que tu sortais comme d'habitude vers 7 h 30 pour te rendre à l'école. C'est la rencontre des deux qui fait le hasard ; elle tombe au moment où tu sortais. Si plusieurs matins de suite, il t'était arrivé la même chose, l'événement n'étant alors plus rare, tu pourrais légitimement penser que ce n'est plus un hasard mais, peut-être, un voisin des étages supérieurs qui t'envoie une tuile et non plus le fait du vent.
J: Fonder l'origine du vivant sur un jeu de hasard a-t-il des conséquences ?
Quand les choses adviennent, il y a plus de détermination que d'indétermination. Les éléments n'existent pas en dehors d'un sujet.
Fonder l'origine du vivant sur un jeu de hasard est une pensée matérialiste, qui suppose une matière éternelle qui détient l'existence par elle-même : une divinisation de la nature. Une croyance !
La théorie de l'évolution est fondée là-dessus. Les êtres qui ont « tirés les bons numéros », les « plus aptes », les « plus forts », sont destinés à supplanter les autres. De nombreuses idéologies mortifères du XX e siècle ont trouvé leur assise sur ce socle de pensée.
Ce socle conceptuel a été souvent promu par des personnes voulant trouver une alternative à la vision chrétienne de l'univers et supprimer Dieu d'une pensée strictement rationnelle [1] . Pourtant, le dualisme ontologique d'un Être, Dieu, distinct de sa création, comporte de nombreuses analogies avec ce que nous observons : l'artiste distinct de son œuvre ; le concepteur de jeux vidéo du jeu de plateforme codé sur ordinateur ; l'artisan de son ouvrage... Il est bien regrettable que Dieu soit systématiquement rejeté comme « fait religieux » alors que la réalité de son existence est attestée, par ailleurs, par de nombreux faits [2] que tout homme de bonne volonté peut constater.
Qui peut donner d'exister sinon Celui qui possède l'existence par Son essence.
La pensée chrétienne est, elle, source de Paix. Il serait absurde de penser qu'un concepteur élabore une création comportant des êtres libres pour qu'ils la détruisent et s'entretuent. Il ne serait pas Amour. L'homme a été établi dans le Jardin pour le cultiver et le garder nous dit la Parole de Dieu [ Gn 2, 15]. Le problème du mal que nous observons a bien une cause, mais c’est un autre sujet.
J : Car nous voilà bien loin de nos protéines !
L : Pas si loin. Les protéines sont des outils primordiaux du vivant et nous avons commencé à voir toute la prédétermination qui existait dans sa fabrication. Le contraire du hasard.
J : Nous en étions arrivés au stade où, grâce à plus d'une centaine de protéines différentes, une information génétique donnait une protéine.
L : Pas exactement. Si nous prenons l'exemple de l'insuline nous n'avons encore qu'une pré-pro-protéine.
J : Peux-tu expliquer ?
L : Après la traduction, toujours pas d’insuline !
Le préfixe « pré » indique la présence d’un « peptide signal ».
Le peptide signal est une séquence d’adressage et d’accrochage qui indique vers quel organite de la cellule le nouveau produit doit être acheminé. Il permet à la protéine SRP (protéine de reconnaissance du signal) de véhiculer le complexe ribosomes, ARNt, facteurs associés et peptide néosynthétisé vers la bonne destination : dans notre cas le réticulum endoplasmique granuleux ( REG ). Le hasard a bien du mal ici à trouver sa place !
L’insuline étant une hormone faite pour être excrétée, elle doit entrer dans le REG .
La séquence signal, ici très hydrophobe, contribue à cet acheminement.
Au fur et à mesure de la traduction, les pièces assemblées franchissent par de petits canaux le seuil de REG. Sur le site d’ancrage, le peptide signal est coupé par l'action d'une enzyme, la signal peptidase . Dorénavant, notre polypeptide ne comporte plus que 86 acides aminés : la pro-insuline.
J : Ce signal peptidase est comme un ciseau ?
L : Oui ! mais il n'est pas spécifique à l'insuline et coupe toujours au bon endroit.
J : Nous avons maintenant une pro-insuline. Ce n'est donc pas encore fini ?
L : Non ! et ce qui vient est à y bien réfléchir assez merveilleux : la mise en forme par soudure et découpage et la formation de deux protéines (ou polypeptides) potentiellement actives différentes.

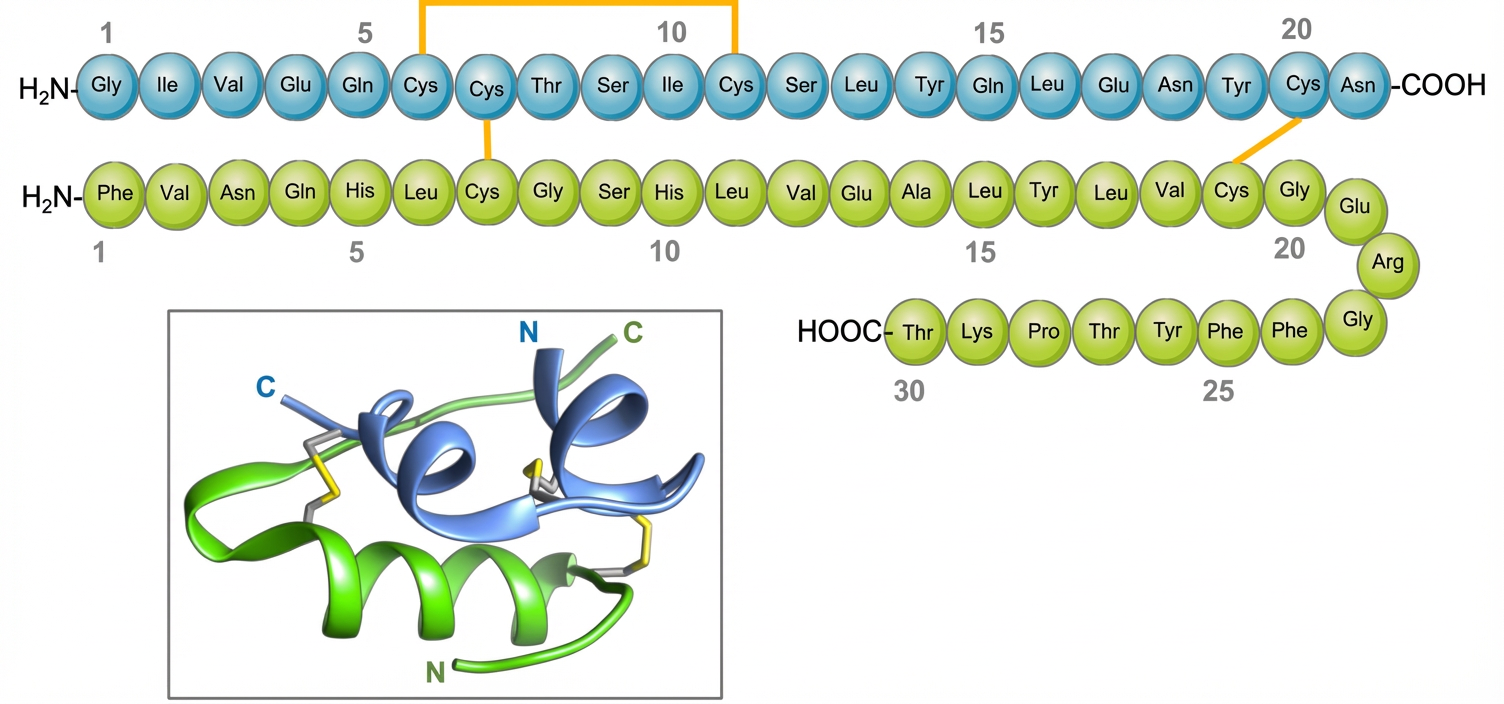
Séquence des 110 acides aminés de la pré-pro-insuline humaine, surlignée selon leurs propriétés. Séquence signal (24 aa); la chaîne β (jaune ; 30 aa); la protéine C (gris ; 31 aa) ; la chaîne α (jaune ; 21 aa). L'insuline est surlignée en jaune. Les acides aminés de propriétés semblables ont la même couleur : Acides aminés basiques, chargés + à pH 7 ; Acides aminés acides chargés - à pH 7 ; Acides aminés polaires non chargés (dont la cystéine en italique) ; Acides aminés apolaires ou hydrophobes. Quatre acides aminés sont éliminés aux sites de coupure.
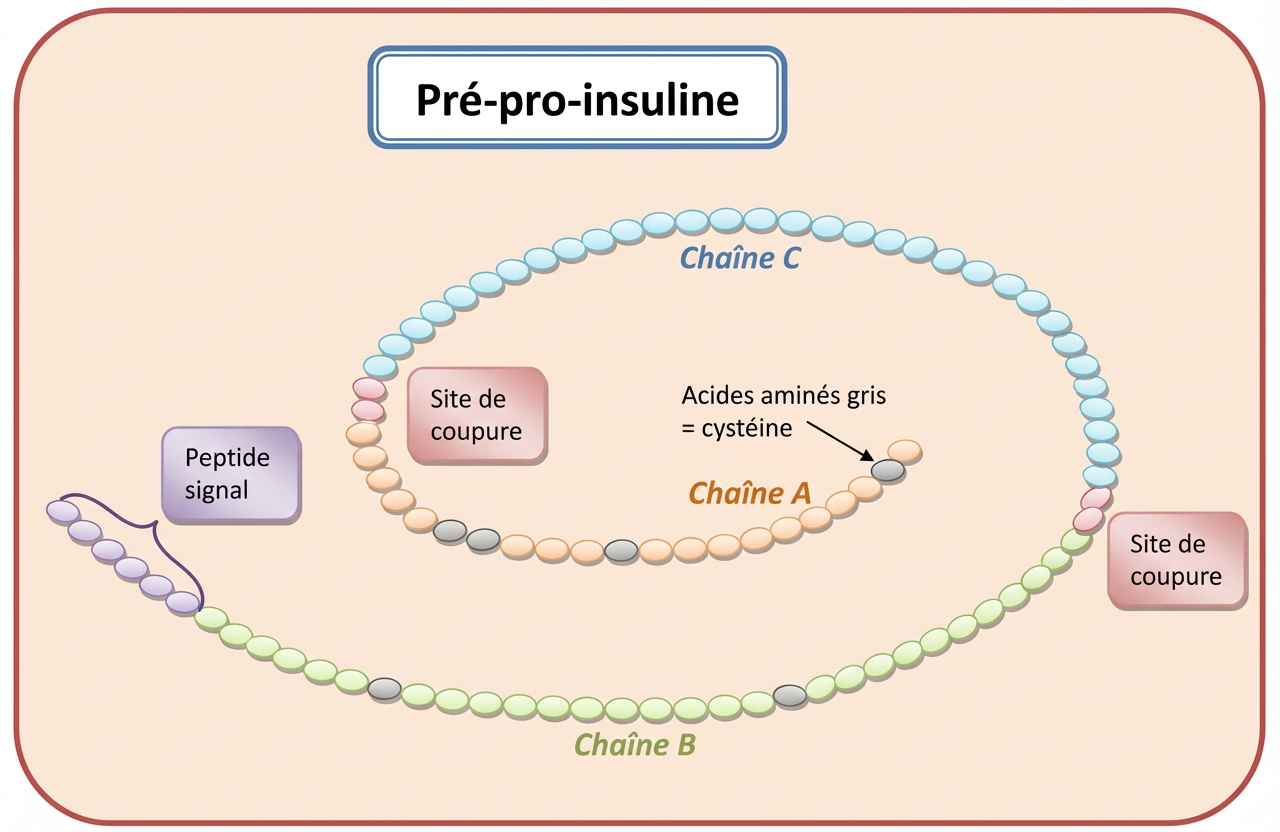
La pré-pro-insuline. E n bleu le peptide C ; en jaune et vert, les deux chaînes de l'insuline qui vont se lier au niveau des acides aminés « cystéine » représentés en gris. Les acides aminés fixant les enzymes de découpe sont en rose et le peptide signal en violet.
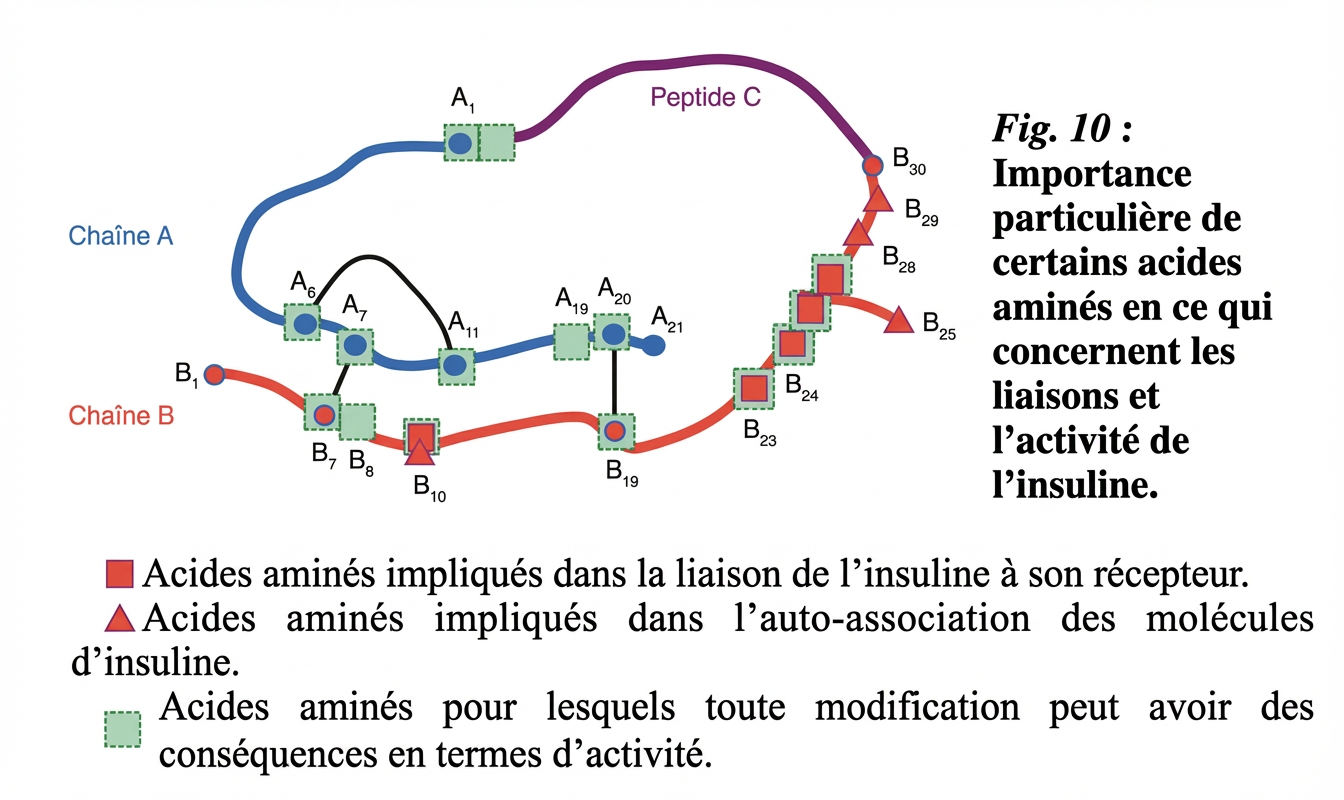
Le REG constitue un environnement plus oxydant que le cytosol [3] . Ce n’est pas sans importance : c’est le « climat » idéal pour la formation des ponts disulfure entre les atomes de soufre de la Cystéine (C) [4] . Ces liaisons fortes, covalentes, sont établies entre la chaîne β et la chaîne α [C31-C96 ; C43-C109] ( cf. Fig. 4 et 5 ). La distance entre les 2 carbones α de 2 résidus cystéine impliqués dans un pont disulfure est de 4,2 Å [ Angström 1 Å= 10 -10 mètre, taille de l’Hydrogène ].
Si on ne connaît pas les règles exactes qui régissent la sélection de telle ou telle cystéine d'une protéine pour établir un pont disulfure, la proximité et les propriétés physico-chimiques des résidus [5] proches sont impliquées (par exemple, la présence d'acides aminés hydrophobes est défavorable à la formation d'un pont disulfure).
Le milieu oxydant ne suffit pas à faire la liaison ; il faut un reploiement de la protéine qui rapproche les cystéines.
Le peptide C ou « peptide de connexion » présente, d’une espèce à l’autre, une plus grande variabilité de composition que l'insuline, mais il facilite dans tous les cas le repliement correct du produit en rapprochant les cystéines de la chaîne par la formation d’un coude (les Prolines : P et les Glycines : G y contribuent).
En se fondant sur les données contemporaines, il s'avère que le peptide C , 31 acides aminés, n’est pas si inactif biologiquement qu’on le croyait au début. Ce n'est pas un simple déchet . Outre son rôle pendant la biosynthèse de l’insuline, il apparaît comme étant une hormone peptidique active (!) [6] qui se lie à un récepteur membranaire couplé aux protéines G, activant ensuite des voies de signalisation intracellulaires calcium-dépendantes. Le résultat final est la potentialisation de l’activité de la pompe sodium-potassium.
Cela est à noter, car si on compare les séquences de différentes espèces allant des Poissons à l’Homme en passant par les Amphibiens, Oiseaux, Mammifères, on remarque ceci :
comme pour le peptide signal, les différences de séquences sont plus substantielles au niveau du Peptide C que celles des chaînes de l’insuline. Il y a donc un taux de variabilité plus ou moins élevé selon les zones du gène ! Hasard ? On peut en douter.
quant à l’insuline, si l’architecture générale est conservée partout , les zones de variabilités ne sont pas indifférentes. L’image du trousseau de clés vient à l’esprit : même si une clé entre dans la serrure, il n’est pas dit qu’elle puisse ouvrir !

Trousseau de clés . Il n'est pas dit que n'importe quelle insuline puisse actionner le récepteur. Les clés d'appartements d'un immeuble se ressemblent, mais n'actionnent chacune que la serrure adaptée.
J: Et la découpe ?
La suppression du peptide C permet l’établissement d’une nouvelle liaison forte au niveau de la chaîne α [ pont disulfure C95-C100 ].
Le clivage de la pro-insuline est catalysé par des enzymes, deux machines spécifiques de découpe : les proconvertases et les carboxypeptidase s. Ces dernières ont une localisation très stricte au sein de la cellule eucaryote et de ses compartiments, ce qui fait qu'elles interviennent au bon moment.
La découpe se fait toujours au niveau de deux paires d’acides aminés basiques qui sont éliminés. Elles sont composées d’Arginine et de Lysine, des acides aminés à longue chaîne chargés positivement : caractéristiques idéales pour fixer les enzymes de passage .
Lors du clivage, les vésicules, qui contiennent insuline et peptide C, perdent leur revêtement de clathrine et deviennent des vésicules matures lisses. L’exocytose se fera au moyen de protéines dites SNARE.
Cette maturation par l'élimination du peptide C retarde la finition du produit et l'apparition de l'activité hormonale de l'insuline, jusqu'à ce qu'elle soit empaquetée dans les granules de sécrétion par sac de six unités liées par deux atomes de zinc à l'intérieur de la cellule β du pancréas.
Lorsqu’une hyperglycémie est signalée, une cosécrétion équimolaire d’insuline et du peptide C est libérée dans le sang. Après bien des péripéties, l’insuline acquiert donc sa forme native, fonctionnelle, juste avant l’exocytose.
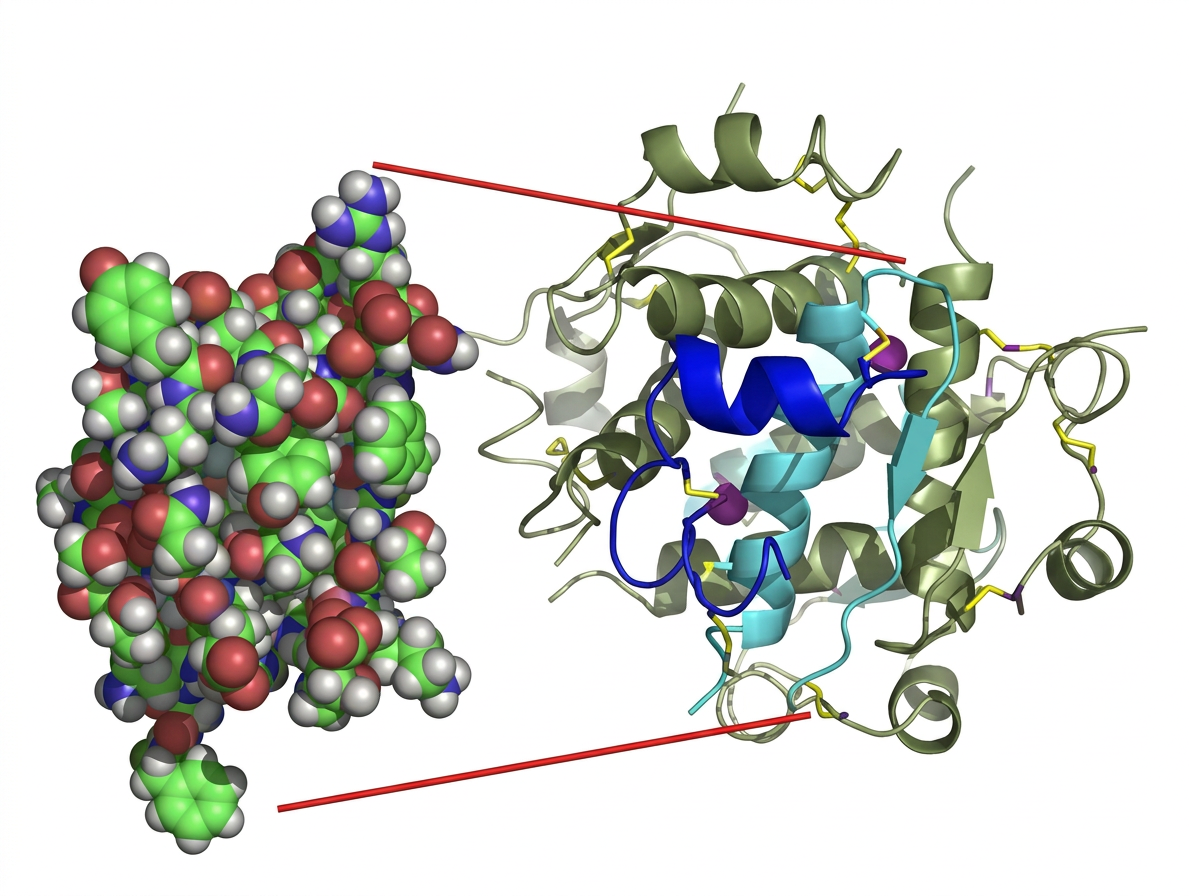
Hexamère d'insuline. Monomère d'insuline en bleu ; Zinc en violet.
J: À quoi servent les atomes de zinc ?
L : Comme le corps fabrique aussi une enzyme de dégradation de l’insuline, la libération sous forme d'hexamères évite une dégradation trop rapide qui ne lui laisserait pas le temps d'agir. La demi-vie de l’insuline est courte : environ 4 heures. L'industrie pharmaceutique tâche, elle, d'avoir des insulines à effet prolongé par des modifications ciblées que l'on ne retrouve pas dans la nature [7] .
J: Mais comment agit l'insuline ?
L: Voilà donc notre insuline, propulsée par le débit sanguin à travers artérioles et artères. À quoi va-t-elle servir ? Si elle n’a pas de récepteur – une structure dans laquelle sa forme lui permet de s’emboîter –, elle ne sera d’aucune utilité !
Il ne sert à rien d’avoir en catalogue l’information permettant sa fabrication si on n’a pas celle de son récepteur et de tous les autres acteurs de la réponse régulatrice de la glycémie. Et ils sont nombreux ! Le récepteur ne fait office que de second messager : c’est la sonnette qui réveille toute une machinerie cellulaire composée d’autres protéines. Codé, lui, sur le chromosome 19, il est d’un tout autre gabarit que la modeste insuline. Il est constitué de 4 peptides glycosylés reliés par des ponts disulfures. Ils forment une énorme glycoprotéine de 400 kDa alors que l’insuline ne fait que 5 808 Da [8] .
J : Le récepteur spécifique n'est donc pas le seul à être indispensable !
L : Exact ! Mais j'aurais bien d'autres choses à te dire sur le récepteur, sa répartition diverse selon les zones du corps, son affinité à l'insuline… mais je ne veux pas te noyer sous les informations. Retiens que l’insuline est comme une prise de courant à connexions multiples ou un tournevis à embout spécifique.
En se fixant, cet outil-prise est responsable de la transduction d’un signal qui, in fine , fait entrer et stocker du glucose.

L’insuline est comme un tournevis à embout spécifique.
Sans récepteur intègre et efficace, l’insuline est inutile, quel que soit son niveau. Il en est de même de tous les acteurs du processus.
J: Si elle ne faisait pas stocker le glucose, qu'adviendrait-il ?
L : Une hyperglycémie. L’insuline est la seule hormone qui permette de faire baisser le taux de sucre présent dans le sang, en favorisant :
Soit son stockage au niveau du foie et du muscle sous forme de glycogène, de manière à être rapidement utilisable. Pour cela il y a mille fois plus de récepteurs à l’insuline sur une cellule musculaire que sur un globule rouge.
Soit son stockage dans le foie et le tissu adipeux pour constituer des réserves sous forme de graisses. Un adipocyte contient 10 000 récepteurs à sa surface à un instant t et, sans son ligand, la demi-vie de ceux-ci est de l’ordre de 7 h.
Normalement, après un repas, lorsque la glycémie augmente, les cellules bêta du pancréas libèrent des hexamères d'insuline à partir de granules de sécrétion dans le sang. On pense que ces hexamères se dissocient rapidement en dimères, puis en monomères lors de la dilution dans le sang, avant que l'hormone puisse se lier au récepteur et exercer ses effets sur les cellules cibles. Les monomères d’insuline et, dans une certaine mesure, les dimères, sont suffisamment petits pour diffuser, à travers les jonctions paracellulaires (c’est-à-dire les jonctions adhérentes), dans le tissu environnant et se lier aux récepteurs à l’insuline situés à la surface des muscles et des cellules adipeuses.
J : Il y a un taux de glycémie dangereux ?
L : Oui ! et c'est tout le problème des personnes diabétiques tel que l'oncle Henri. Un taux de glycémie trop bas (hypoglycémie) c'est-à-dire inférieur à 0,60 g par litre à jeun ; tout comme un taux de sucre trop élevé (hyperglycémie), c'est-à-dire supérieur à 1,10 g par litre à jeun, est dangereux. Cette régulation est donc nécessaire.
Le diabète est une maladie chronique caractérisée par une hyperglycémie chronique. Les hyperglycémies répétées, prolongées, et le déséquilibre du diabète provoquent une altération des nerfs et des vaisseaux et, par voie de conséquence, une altération de certaines cellules de l'organisme, avec des répercutions sur plusieurs organes.
Le diabète entraîne une augmentation de la mortalité à l’âge adulte, réduisant en moyenne l'espérance de vie de six ans.
D’après le rapport 2019 de la Fédération Internationale du Diabète, 578 millions d'adultes seront atteints de diabète d'ici 2030 et 700 millions d'ici 2045. La production industrielle d'insuline a de beaux bénéfices en perspective.
J : On arrive à la fabriquer ? Mais alors, ne peut-elle pas apparaître spontanément ?
L : Non ! La production industrielle utilise juste les connaissances acquises pour imiter la nature. Dans certains protocoles, pour obtenir la pré-pro-insuline, elle utilise des bactéries pour obtenir la pré-pro-insuline en évitant les étapes d'épissage de l'ARNm, puis elle effectue les mêmes modifications post-traductionnelles que celles observées dans la nature mais cela nécessite beaucoup de matériel.

La production industrielle nécessite beaucoup de matériel.
L'histoire des premières insulines administrées aux diabétiques insulino-dépendants montrent même que ces insulines différant de l'humaine de un ou deux acides aminés, et extraites de pancréas de bœuf ou de porc, étaient responsables de réactions locales ou d’allergies à cause d'une purification imparfaite et de cette différence structurelle . Au début des années 80, on a même décidé de modifier l’insuline porcine.
Par des transformations enzymatiques, on a pu remplacer le seul acide aminé qui différait (alanine chez le porc ; thréonine chez l'homme) : ce fut l'insuline semi-synthétique humaine. Bien qu’apportant au malade une plus grande efficacité, ce procédé nécessitait encore un approvisionnement en insuline porcine et provoquait dans certains cas des réactions de rejet.
Ce simple fait va à l'encontre des phylogénies (lignées évolutives supposée par les évolutionnistes) déduites abusivement des comparaisons de séquences.
Maintenant, avec la technique de l'ADN recombinant et les bactéries, les groupes pharmaceutiques fabriquent différentes variétés d'insuline qui ne se retrouvent pas dans la nature. Le pancréas reste cependant inégalé en termes de temps de production et de miniaturisation de la chaîne de fabrication.
J : Le pancréas ?
L : Je t'ai déjà dit que dans un être vivant, chaque cellule a le même programme génétique, mais elle l’exprime de manière différente. Ainsi toutes les cellules du corps ne fabriquent pas d’insuline. Seules les cellules β des îlots de Langerhans du pancréas s’en occupent. Cette spécialisation résulte de leur histoire. L’environnement de la cellule étant capital pour l’expression génique, l’expression des gènes dans le temps et l’espace entraîne des régionalisations, des différenciations très dépendantes des molécules présentes, de leur concentration et de leur état moléculaire (selon le pH, la température, etc.). Le développement embryonnaire l’illustre parfaitement. C’est le déroulement du programme qui importe .
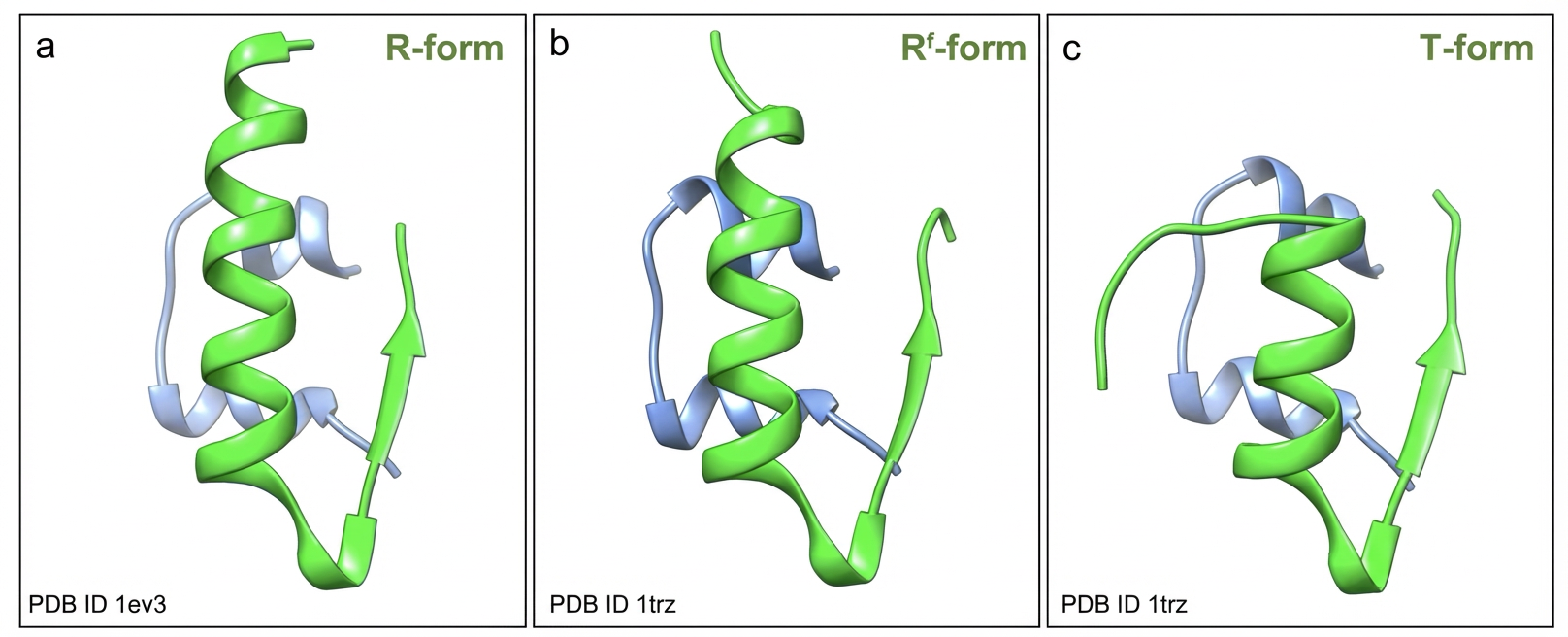
Différentes conformations en hélice de l’insuline mature. Elle montre les « hélices ⍺ » (représentées par la spirale) que la structure primaire fait prévoir : pour que la protéine adopte cette conformation, il faut qu’une portion de la chaîne d’acides aminés soit amphiphile : alternance d’acides aminés hydrophile et hydrophobe . La longueur moyenne d’une hélice est de 10 résidus ce qui correspond à 3 tours environ (3,6 résidus par tour pour un pas de 0,54 nm). Ce sont les liaisons H (hydrogène) orientées entre les groupes fonctionnels NH et CO des liaisons peptidiques qui stabilisent l’hélice. La disposition en « feuillet » est représentée par une flèche, le reste sont des « coudes » (trait fin filiforme) qui relient ces structures. Bien que théoriquement la nouvelle protéine ainsi fabriquée puisse avoir un très grand nombre de conformations possibles, en réalité il n’en existe qu’un petit nombre, du fait des propriétés qu’elle doit présenter [9] .
La cellule productrice d’insuline est comme une usine mesurant 35 μm ou 0,035 mm. Le « complexe industriel » auquel elle appartient s’appelle îlot de Langherans . Il y a, répartis inégalement, entre 750 000 et 1 500 000 complexes de ce genre dans la « ville » Pancréas, mais leur ensemble ne constitue que 1 à 2 % du volume de celle-ci, l’activité principale étant la fabrication, pour la digestion, du suc pancréatique riche en bicarbonates et enzymes.
Le nombre d’usines dans chaque complexe est variable : de quelques-unes pour les plus petits jusqu’à environ 5 000 pour les plus grands. Chez l’homme, l’ Îlot de Langerhans est organisé ainsi : en son centre, des « usines » fabriquant de l’insuline (65-80 % du complexe) [ cellules bêta ] ; en périphérie, des « usines » produisant du glucagon (15-20 % du complexe) [ cellules alpha ], la somatostatine (3-10 %) [ cellules delta ], le polypeptide pancréatique (1 %) [ cellules F ou PP ] ou la ghréline [ cellules epsilon ].
J : Quelle belle organisation ! Oui, papa ! il faut le dire : il est contraire au bon sens de penser que tout cela ait pu se faire par hasard à partir d'une quelconque « soupe primitive » !
_____________________________
Bibliographie complémentaire
Biologie tout-en-un - BCPST 1 ère année - P. PEYCRU, D. GRANPERRRIN & C. PERRIER, Paris, Dunod, 2017.
https://sciencedirect.com/science/article/abs/pii/S1957255721001784
Uniprot.org : INS, reviewed, nom du gène.
http://education.expasy.org/bioinformatique/journee_diabete.html
Cet article est publié par le Centre d'Études et de Prospective (CEP)
Voir l'article sur le site